| 2006 corrigé : combustion d'un hydrocarbure dans le dioxygène |
|
Vous êtes ici : Hydrocarbures > 2006 : Combustion d'un hydrocarbure dans le dioxygène
2.1 l'équation équilibrée de la réaction de combustion dans
CH
2.2 - a) La quantité de matière de dioxygène utilisée.
CH
b) La quantité de matière du composé CH
n
c) La masse du composé CH
m
n
M
m
|

 + 2 O
+ 2 O 2 H
2 H O + CO
O + CO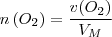

 =
=  = 2 mol
= 2 mol M
M


 -
Avenue Bourguiba x rue 14 Castors, Dakar (Sénégal) - Tél/Fax : +221 33864 62 33
-
Avenue Bourguiba x rue 14 Castors, Dakar (Sénégal) - Tél/Fax : +221 33864 62 33